Ministerul Sănătății și Casa Naţională de Asigurări de Sănătate au emis un ordin comun pentru aprobarea protocoalelor terapeutice necesare prescrierii unor medicamente compensate
Ministerul Sănătății și Casa Naţională de Asigurări de Sănătate au emis un ordin comun pentru aprobarea 2158
Marime text
2158
Marime text
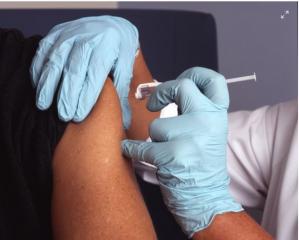
Astfel, prin noile prevederi, pentru inițierea tratamentului specific unei afecțiuni cu medicamente care se eliberează prin farmaciile comunitare, medicii pot opta pentru prescrierea unui produs biosimilar. Totodată, pentru continuarea tratamentului specific pentru care, la momentul prescrierii, există atât produsul biologic de referinţă, cât și produsul biosimilar, se recomandă schimbarea produsului original cu un biosimilar al acestuia.
La iniţierea sau schimbarea tratamentului cu un medicament biosimilar, medicul curant va prezenta pacientului cea mai bună opţiune pentru acesta și va prescrie medicamentul biosimilar numai după obținerea consimțământului informat al pacientului. Aceste prevederi au scopul de a extinde accesul la opțiuni terapeutice și nu obligă medicii să prescrie un anumit tip de medicament.
„Produsele biosimilare sunt certificate prin studii care indică faptul că au aceleaşi efecte cu produsele biologice de referinţă și nu există diferenţe semnificative clinic între cele două în ceea ce priveşte siguranţa, calitatea şi eficacitatea. Prin utilizarea medicamentelor biosimilare creștem accesul pacienților la tratamentul de care au nevoie. Prin această abordare, statul poate să trateze mai mulți pacienți cu aceleași fonduri și creștem numărul de medicamente disponibile, fără a afecta eficacitatea tratamentului”, a declarat ministrul Sănătății, Ioana Mihăilă.
„Măsuri asemănătoare de adopție a medicamentelor biosimilare în terapia recomandată de către medicii prescriptori au fost luate de majoritatea statelor Uniunii Europene, în vederea eficientizării fondurilor disponibile alocate sănătății care să permită un acces mai amplu al pacienților la tratamentul necesar. CNAS va continua și intensifica dialogul cu toți partenerii instituționali pentru identificarea celor mai potrivite soluții, inclusiv din experiența altor țări europene, care să crească accesul pacienților la tratamente sigure și eficiente și să îmbunătățească permanent eficiența utilizării Fondului Național Unic de Asigurări Sociale de Sănătate”, a declarat președintele CNAS, Adrian Gheorghe.
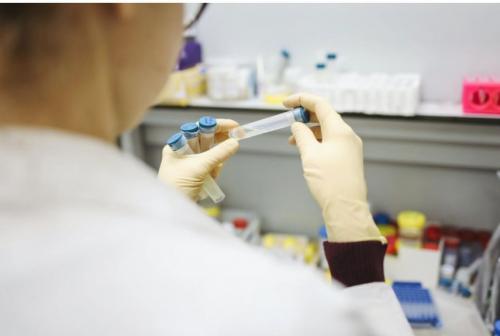
*Potrivit Agenției Europene pentru Medicamente (EMA), medicamentele biologice conțin substanțe active provenite dintr-o sursă biologică, de exemplu din celule sau organisme vii. Medicamentele biologice au o utilizare bine stabilită în practica clinică, fiind în multe cazuri indispensabile pentru tratamentul unor afecțiuni grave și cronice, precum diabetul sau diferitele tipuri de boli autoimune și de cancer.
Un medicament biosimilar este un medicament înalt similar cu un alt medicament biologic deja comercializat în UE (cunoscut ca „medicament biologic de referință”). Companiile pot primi aprobarea de punere pe piață a medicamentelor biosimilare după expirarea perioadei de protecție pe piață a medicamentului de referință (aproximativ 10 ani). Deoarece medicamentele biosimilare sunt un tip de medicamente biologice, li se aplică toate caracteristicile relevante ale medicamentelor biologice. Având în vedere variabilitatea naturală a sursei biologice și faptul că fiecare producător aplică un proces de fabricație diferit, pot apărea diferențe minore între medicamentul biosimilar și medicamentul său de referință. Medicamentele biosimilare sunt aprobate în conformitate cu aceleași standarde de calitate farmaceutică, siguranță și eficacitate aplicate tuturor medicamentelor biologice aprobate în UE.
Urmareste-ne pe Grupul de Whatsapp
 Fondul Documentar Dobrogea de ieri și de azi
Fondul Documentar Dobrogea de ieri și de azi